Theo Heidi Ledford(2021). COVID vaccines and blood clots: what researchers know so far. doi: https://doi.org/10.1038/d41586-021-02291-2
Ngày đăng: 24/08/2021
Vui lòng ghi rõ nguồn https://cnsh.vnua.edu.vn/ khi đăng lại nội dung này
Các nhà khoa học đang cố gắng tìm hiểu lý do một số ít người gặp chứng rối loạn đông máu sau khi tiêm vaccine Covid. Đông máu thường ít gặp ở lứa tuổi trẻ và càng hiếm khi đi kèm với hiện tượng giảm tiểu cầu ở mức báo động. Đến nay, có hai bệnh nhân trẻ gặp hiện tương này sau khi tiêm vaccine AstraZeneca.
Nicolson, một chuyên gia huyết học, đã chứng kiến tình trạng giảm tiểu cầu huyết khối miễn dịch do vaccine (VITT), một tình trạng nguy hiểm và khó hiểu ảnh hưởng đến một số rất nhỏ những người đã được tiêm vaccine AstraZeneca hoặc Johnson & Johnson (J&J). Ước tính rằng cứ 50.000 người dưới 50 tuổi sẽ có một người gặp phải VITT sau khi tiêm vaccine AstraZeneca
Mặc dù sự liên quan giữa vaccine và VITT vẫn chưa rõ ràng nhưng cần nhanh chóng tìm ra các biện pháp ngăn ngừa và điều trị tình trạng này, đồng thời cải tiến các vaccine hiện có.
Các khái niệm về đông máu
Các triệu chứng hiếm gặp trên không còn mới mẻ với các nhà huyết học trong điều trị các bệnh nhân có phản ứng lạ khi dùng thuốc chống đông heparin (hôi chứng HIT). HIT gây ra bởi heparin, liên kết với yếu tố tiểu cầu 4 (PF4) được sản xuất bởi tiểu cầu để thúc đẩy quá trình đông máu. Ở một số người, hệ thống miễn dịch coi phức hợp này là ngoại lai và phát triển các kháng thể chống lại nó. Các kháng thể này cũng có thể liên kết và làm tiểu cầu kết tụ lại với nhau và kích hoạt quá trình đông máu. Các cục máu đông làm tắc nghẽn các mạch máu quan trọng dẫn tới tử vong.
Việc phân tích cho thấy những người tiêm vaccine có phản ứng đông máu cũng tạo ra kháng thể chống lại PF42-4 của chính họ. Kelton, người đã nghiên cứu HIT lâu năm nhận thấy khoảng 2/3 số mẫu không có kháng thể PF4, tức là các bệnh nhân không bị VITT mà mắc phải một chứng rối loạn đông máu có thể không liên quan đến việc tiêm chủng của họ. Khi nhóm của ông nghiên cứu năm mẫu bệnh phẩm từ những người trước khi điều trị VITT, họ xác định đặc điểm của các kháng thể trong các mẫu và phát hiện một số liên kết với PF4 tại cùng vị trí với chất được sử dụng bởi heparin và chúng cũng có khả năng kích hoạt tiểu cầu[5]. Kết quả cho thấy cơ chế của hội chứng liên quan đến vaccine tương tự như cơ chế của HIT - nhưng tác nhân gây ra dường như là vaccine.
Nghiên cứu về các thành phần trong vaccine
VITT có liên quan đến hai loại vaccine COVID-19 đều sử dụng adenovirus bất hoạt làm vector để đưa gen mã hóa protein gai của SARS-CoV-2 vào cơ thể. Sau đó, gen được biểu hiện và tạo ra protein, kích thích hệ miễn dịch tạo ra các kháng thể, yếu tố quan trọng để chống lại sự lây nhiễm coronavirus.
Một số nhà nghiên cứu cho rằng các tạp chất trong vaccine còn sót lại từ quá trình sản xuất tương tác với PF4 để tạo ra các khối bị tấn công bởi kháng thể[6]. Một số người nghĩ rằng thủ phạm có thể là chính adenovirus, chúng liên kết với tiểu cầu và kích hoạt sự suy giảm tiểu cầu ở chuột[7].
    |
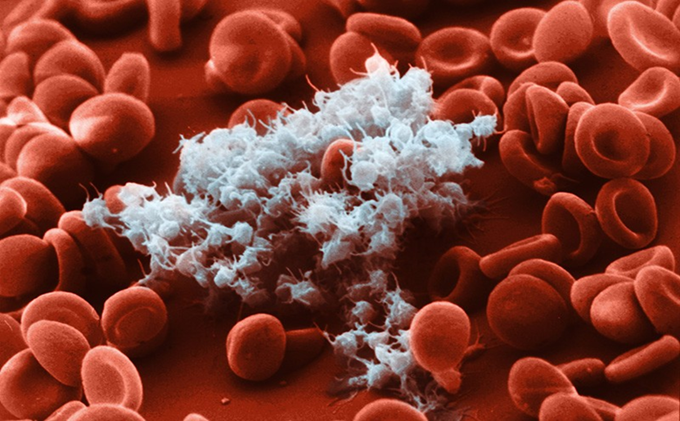 |
| Tiểu cầu (màu trắng) là những mảnh tế bào kích thích hình thành cục máu đông. Nguồn: Lennart Nillson, Boehringer Iingelheim International |
Trước đại dịch COVID-19, vaccine dựa trên adenovirus dùng để chống lại HIV và Ebola nhưng vẫn chưa được sử dụng trên rộng rãi như vaccine Astra Zeneca và cũng, không có báo cáo nào cho thấy những vaccine này gây ra tình trạng giống VITT.
Nhà huyết học Mitesh Borad và cộng sự đã phân tích cấu trúc của adenovirus ở tinh tinh được sử dụng sản xuất vaccine AstraZeneca. Mang điện tích âm mạnh cho phép nó liên kết với protein PF4[8] tích điện dương. Nó có thể tạo ra một chuỗi phản ứng giống như phản ứng hiếm gặp với heparin. Một số adenovirus có thể được thiết kế để giảm điện tích âm của chúng, và một số ít mang điện tích âm hơn những loại khác. Ví dụ như adenovirus Ad26 được sử dụng trong vaccine J&J không có nhiều tác dụng như virus ở tinh tinh, điều này có thể giải thích tại sao VITT dường như ít phổ biến hơn ở những người tiêm J&J. Vaccine của Oxford – AstraZeneca và các vaccine khác dựa trên adenovirus khác có thể an toàn hơn nếu các protein gai của chúng được thiết kế tương tự như J&J. Cho đến nay, không có mối liên quan nào giữa VITT và vaccine Sputnik V, loại sử dụng cả Ad26 và một loại virus adenovirus Ad5 ít mang điện tích âm hơn. Thay vì dừng sử dụng adenovirus, chúng ta nên nghĩ cách phát triển chúng một cách an toàn và nghiên cứu thêm về các phản ứng miễn dịch đối với chúng.
Ngoài ra, có nghi vấn cho rằng các kháng thể liên kết với PF4 ở những người bị VITT là do phản ứng miễn dịch của cơ thể đối với protein gai. Nhưng họ phát hiện ra rằng các kháng thể PF4 không thể liên kết với protein gai, chứng tỏ rằng chúng không phải là kết quả của phản ứng miễn dịch với protein virus[9].
Tuy nhiên, các đoạn RNA mã hóa cho protein gai có thể được cắt rời và nối lại với nhau theo nhiều cách khác nhau, tạo ra các protein gai đi vào máu và sau đó liên kết với bề mặt của các tế bào trên mạch máu[10]. Ở đó, chúng gây ra phản ứng viêm ở một số bệnh nhân SARS-CoV-2, những người nhiễm bệnh nặng có thể hình thành các cục máu đông.
Một yếu tố có thể giảm sự an toàn của vaccine từ adenovirus là do cách sử dụng. Vaccine COVID-19 được tiêm vào cơ nhưng nếu kim đâm vào tĩnh mạch, vaccine có thể đi trực tiếp vào máu. Các tiểu cầu đã phát hiện có sự kết tụ với adenovirus khi vaccine AstraZeneca được tiêm vào mạch máu[12]. VITT có thể được phòng tránh bằng cách yêu cầu người tiêm chủng hút tiến hành thêm một thao tác hút một lượng nhỏ chất lỏng từ vị trí tiêm bằng ống tiêm để kiểm tra ttrước khi họ thực hiện tiêm. Đây là thao tác tiêu chuẩn được thêm vào hướng dẫn chính thức về tiêm vaccine COVID-19 ở Đan Mạch và một số quốc gia.
Cải tiến các phương pháp điều trị
Hiện tại VITT được điều trị bằng các phương pháp chống đông máu mà không dùng tới heparin và sử dụng liều lượng cao các kháng thể tự nhiên từ người hiến huyết tương. Kháng thể tự nhiên cạnh tranh với kháng thể kháng PF4 để tìm vị trí gắn kết trên tiểu cầu, làm giảm nguy cơ đông máu.
Tại Birmingham, Nicolson đã xét nghiệm huyết thanh của những người mắc VITT để xem liệu có thể sử dụng lại các loại thuốc dành cho các tình trạng khác để điều trị nó hay không. Đặc biệt, ông đang tập trung vào các phương pháp điều trị can thiệp vào protein trên tiểu cầu để tìm loại thuốc có thể ngăn chặn sự kích hoạt tiểu cầu và các phản ứng hình thành cục máu đông trong VITT.
Kể từ khi ghi nhận những trường hợp đầu tiên vào tháng 3 năm nay, nước Anh đã thay đổi chính sách tiêm chủng và khuyến cáo chỉ tiêm vaccine AstraZeneca cho những người trên 40 tuổi. VITT thường xảy ra hơn ở bệnh nhân trẻ, có thể vì họ có phản ứng miễn dịch mạnh hơn.
Không rõ liệu các quốc gia khác có quan tâm tới việc hạn chế tiêm vaccine AstraZeneca cho người lớn tuổi hay không. Cho đến nay, VITT chủ yếu được ghi nhận ở Châu Âu và Hoa Kỳ, nhưng các nhà nghiên cứu vẫn chưa biết điều này phản ánh sự khác biệt giữa các khu vực về tính nhạy cảm với VITT hay sự khác biệt trong hệ thống thu thập dữ liệu về các tác dụng phụ tiềm ẩn của vaccine. Số lượng người nhập viện vì VITT đã giảm đáng kể, tình trạng này gần như đã ngừng xảy ra.
Người dịch: Nguyễn Thị Thanh Mai
Biên tập: CTTT, NVK
Tài liệu tham khảo:
1. Pavord, S. et al. N. Engl. J. Med. https://doi.org/10.1056/NEJMoa2109908 (2021).
2. Schultz, N. H. et al. N. Engl. J. Med 384, 2124–2130 (2021).
3. Greinacher, A. et al. N. Engl. J. Med. 384, 2092–2101 (2021).
4. Scully, M. et al. N. Engl. J. Med. 384, 2202–2211 (2021).
5. Huynh, A., Kelton, J. G., Arnold, D. M., Daka, M. & Nazy, I. Nature https://doi.org/10.1038/s41586-021-03744-4 (2021).
6. Greinacher, A. et al. Preprint at Research Square. https://doi.org/10.21203/rs.3.rs-440461/v1 (2021).
7. Othman, M., Labelle, A., Mazzetti, I., Elbatarny, H. S. & Lillicrap, D. Blood 109, 2832–2839 (2007).
8. Baker, A. T. et al. Preprint at bioRxiv. https://doi.org/10.1101/2021.05.19.444882 (2021).
9. Greinacher, A. et al. Blood. https://doi.org/10.1182/blood.2021012938 (2021).
10. Kowarz, E. et al. Preprint at Research Square https://doi.org/10.21203/rs.3.rs-558954/v1(2021).
11. Nicolai, L. et al. Preprint at bioRxiv https://doi.org/10.1101/2021.06.29.450356 (2021).