Theo Smriti Mallapaty “India’s DNA COVID vaccine is a world first – more are coming”
Nature 597, 161-162 (2021) doi: https://doi.org/10.1038/d41586-021-02385-x
Ngày đăng: 2/9/2021
Vui lòng ghi rõ nguồn https://cnsh.vnua.edu.vn/ khi đăng lại nội dung này
Vaccine ZyCoV-D dự báo có một làn sóng vaccine DNA cho các nhiều loại bệnh khác nhau đang được thử nghiệm lâm sàng trên khắp thế giới.
Ấn Độ đã phê duyệt một loại vaccine COVID mới, sử dụng chuỗi DNA dạng vòng giúp hệ miễn dịch chống lại virus SARS-CoV-2. Các nhà nghiên cứu hi vọng loại vaccine DNA đầu tiên được chấp thuận rộng rãi trên thế giới và cho biết nhiều loại vaccine DNA khác có thể sẽ sớm xuất hiện sau đó.
ZyCoV-D, loại vaccine được tiêm trong da mà không cần kim tiêm, có khả năng bảo vệ đến 67% chống COVID-19 trong các thử nghiệm lâm sàng. Vaccine DNA này có thể bắt đầu được sử dụng ở Ấn Độ trong tháng này. Mặc dù hiệu quả không đặc biệt cao so với nhiều loại vaccine COVID-19 khác, nhưng đây loại vaccine DNA đầu tiên được sử dụng. Đây là một bước tiến thực sự quan trọng trong cuộc chiến đánh bại COVID-19 trên toàn cầu, nếu vaccine DNA được chứng minh thành công, đây sẽ thực sự là tương lai của công nghệ tiêm chủng vì chúng rất dễ sản xuất.
    |
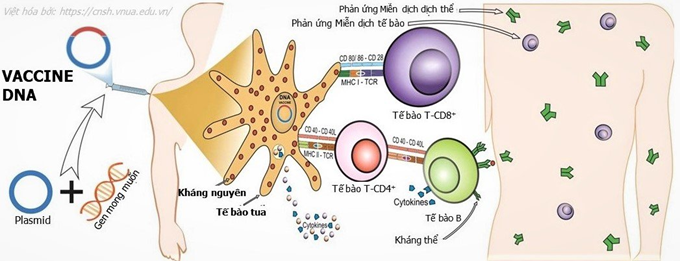 |
| Cơ chế tạo miễn dịch của Vaccine DNA |
Phát triển nhanh chóng
Tính cấp bách của cuộc chiến chống COVID-19 đã đẩy nhanh sự phát triển của vaccine sử dụng kỹ thuật di truyền như vaccine RNA và DNA. Vaccine RNA nhanh chóng tạo ra các phản ứng miễn dịch mạnh mẽ nhưng vaccine DNA lại có có nhiều lợi ích hơn như dễ sản xuất, thành phẩm ổn định so với vaccine mRNA yêu cầu bảo quản ở nhiệt độ rất thấp.
ZyCoV-D được phát triển bởi công ty dược phẩm Ấn Độ Zydus Cadila, có trụ sở chính tại Ahmedabad. Ngày 20 tháng 8, cơ quan quản lý dược phẩm của Ấn Độ đã cho phép tiêm vaccine này cho người từ 12 tuổi trở lên. Tỷ lệ hiệu quả đạt 67% với hơn 28.000 người, trong thử nghiệm có 21 trường hợp có triệu chứng nhiễm COVID-19 thuộc nhóm được tiêm vaccine so với 60 trường hợp thuộc nhóm dùng giả dược.
ZyCoV-D chứa các plasmid mã hóa cho protein gai của SARS-CoV-2, cùng với một trình tự mở đầu để kích hoạt gen. Khi các plasmid đi vào nhân tế bào, chúng sẽ được phiên mã thành mRNA, đi ra tế bào chất và được dịch mã thành protein gai. Sau đó, hệ miễn dịch của cơ thể nhận biết và kích hoạt phản ứng chống lại protein gai, tạo ra các tế bào miễn dịch ghi nhớ dài hạn. Plasmid trong vaccine đưa vào cơ thể thường bị suy giảm sau vài tuần đến vài tháng.
Vaccine DNA và mRNA đã được phát triển từ những năm 1990. Nhược điểm của vaccine DNA là chúng cần phải tới tận nhân tế bào, không giống như vaccine mRNA, chỉ cần đến tế bào chất. Vaccine DNA cần thời gian dài để tạo ra các phản ứng miễn dịch rõ ràng trong thử nghiệm lâm sàng, đó là lý do tại sao cho đến nay chúng chỉ được cấp phép cho tiêm trên cho động vật, chẳng hạn như ngựa.
Vaccine không cần mũi tiêm
ZyCoV-D được tiêm trong da, khu vực có nhiều tế bào miễn dịch thực bào các hạt vaccine và xử lý chúng, giúp thu nhận DNA hiệu quả hơn so với tiêm vaccine vào bắp. Khác với thông thường, vaccine này sử dụng “bơm tiêm không có kim tiêm” ép vào da, tạo ra một dòng chất lỏng nhỏ, áp suất cao đi qua bề mặt và ít đau hơn so với tiêm.
Mặc dù mạnh hơn các vaccine DNA trước đây, ZyCoV-D khuyến cáo tiêm tối thiểu ba mũi để đạt được hiệu quả miễn dịch. Điều này có thể làm tăng thêm thách thức trong việc vận chuyển và dự trữ vaccine.
Mặc dù hiệu quả của ZyCoV-D có vẻ thấp so một số vaccine mRNA nhưng các số liệu này không thể so sánh với nhau được. Vì các thử nghiệm ZyCoV-D ở Ấn Độ được tiến hành khi biến thể Delta đang hoành hành, trong khi các vaccine mRNA trước đó được thực hiện khi có ít các biến thể lây lan mạnh như Delta. Những liều vaccine đầu tiên sẽ được tiêm ở Ấn Độ vào tháng 9 và 50 triệu liều được lên kế hoạch sản xuất vào đầu năm tới.
Các loại vaccine DNA đang thử nghiệm lâm sàng
Nhiều loại vaccine DNA COVID-19 đang được thử nghiệm lâm sàng trên thế giới.
|
Vaccine
|
Đơn vị phát triển
|
Quốc gia
|
Vị trí
|
Giai đoạn thử nghiệm
|
|
ZyCoV-D
|
Zydus Cadila
|
Ấn Độ
|
Da
|
Được cấp phép khẩn cấp
|
|
INO-4800
|
Inovio and partners
|
Mỹ
|
Da
|
Giai đoạn II/III
|
|
AG0302-COVID19
|
AnGes, Osaka
University, Takara Bio
|
Nhật Bản
|
Cơ
|
Giai đoạn II/III
|
|
GX-19N
|
Genexine
|
Hàn Quốc
|
Cơ
|
Giai đoạn I/II
|
|
GLS-5310
|
GeneOne Life Science
|
Hàn Quốc
|
Da
|
Giai đoạn I/II
|
|
COVID-eVax
|
Takis, Rottapharm Biotech
|
Ý
|
Cơ
|
Giai đoạn I/II
|
|
AG0301-COVID19
|
AnGes, OSaka University, Takara Bio
|
Nhật Bản
|
Cơ
|
Giai đoạn I/II
|
|
Covigenix VAX-001
|
Entos Pharmaceuticals
|
Canada
|
Cơ
|
Giai đoạn I
|
|
CORVax12
|
OncoSec, Providence Cancer Institute
|
Mỹ
|
Da
|
Giai đoạn I
|
|
bacTRL-Spike
|
Symvivo
|
Canada
|
Miệng
|
Giai đoạn I
|
|
COVIGEN
|
BioNet, Technovalia, University of Sydney
|
Thái Lan, Úc
|
Da và cơ
|
Giai đoạn I
|
Nguồn: World Health Organization. COVID-19 Vaccine Tracker and Landscape (WHO, 2021).
Tình hình phát triển Vaccine DNA trên thế giới
Một số vaccine DNA khác cũng đang được phát triển sử dụng nhiều loại kháng nguyên và cơ chế tiêm chủng khác nhau. Hai đơn vị đã đi vào thử nghiệm ở giai đoạn cuối gồm công ty AnGes, Nhật Bản và công ty dược phẩm Inovio, Pennsylvania. Inovio được tiêm dưới da và sử dụng một thiết bị với các xung điện ngắn để tạo các lỗ trong các tế bào nơi vaccine có thể đi qua.
Một số vaccine DNA khác đang được thử nghiệm giai đoạn đầu gồm vaccine của công ty công nghệ sinh học GeneOne Life Science, Hàn Quốc; công ty BioNet của Thái Lan mà Richmond cũng tham gia phát triển. Vaccine DNA cũng đang được phát triển phòng bệnh cúm, virus papilloma ở người, HIV, Zika và cả bệnh ung thư.
Ưu điểm của vaccine DNA là có thể lưu trữ nhiều thông tin và mã hóa cho cùng lúc 1 hoặc nhiều protein, phân tử kháng nguyên lớn và phức tạp hơn. David Weiner, giám đốc trung tâm Vaccine và liệu pháp miễn dịch, Philadelphia, Pennsylvania.cho rằng: “ Đây chính thời điểm mà lĩnh vực kỹ thuật di truyền sẽ lên ngôi, ngành này cuối cùng đã có cơ hội để phát huy khả năng và thế mạnh của mình”
Người dịch: Trương Xuân Anh
Biên tập: CTTT, HHY, NQT